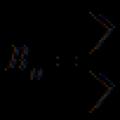«Соль азотной кислоты» - Что получается при разложении нитрата натрия? Физические свойства нитратов. Укажите окислитель, восстановитель. Химические свойства нитратов. Знать и уметь. Раствор азотной кислоты реагирует с каждым из веществ. К каким выводам пришел юный химик? Все нитраты термически неустойчивы. Занимательная история.
«Теории кислот и оснований» - Например, какая кислота сильнее уксусная (СН3СООН или хлоруксусная ClCH2COOH? 2. Реакции присоединения. Силу основанияR3N в воде можно оценить, рассматривая равновесие: Джилберт Ньютон Льюис. Мерой кислотности является константа равновесия, называемая константой кислотности (Ka). Сванте-Август Аррениус.
«Уксусная кислота» - Что такое кислоты? Не во всех фруктах и овощах присутствуют кислоты. Кислоты. В чистом виде муравьиную кислоту впервые получил в 1749г. Андреас Сигизмунд Маргграф. Путешествие в мир кислот. Как обнаружить кислоты? Раствор муравьиной кислоты. История открытия кислот. Кислоты имеют сходный состав. Какие вещества относятся к кислотам?
«Кислотные дожди» - В Балтийском регионе предполагается появление новых озоновых дыр. Алюминий способен вызывать болезнь. Можно предположить, что происходит и с дикими видами животных, когда погибают леса. Нам же, да и почти всему живому нужна вода пресная. Вместе с гибелью озер становится очевидной и деградация лесов.
«Карбоновые кислоты» - Повторите определение карбоновых кислот. Получение карбоновых кислот. Строение карбоксильной группы. Карбоновые кислоты. Что называется карбоновыми кислотами? Номенклатура сложных эфиров. Все карбоновые кислоты имеют функциональную группу. Молекулы карбоновых кислот образуют димеры. Химические свойства карбоновых кислот.
«Нуклеиновые кислоты» - 1892г. – химик Лильенфельд выделил тимонуклеиновую кислоту из зобной железы 1953г. Азотистое основание. Лабораторный практикум. Строение нуклеотидов (отличия). 1868г. - немецкий химик Ф. Мишер открыл нуклеиновые кислоты. Биологическая роль нуклеиновых кислот. Сравнительная характеристика. Длина молекул ДНК (американский биолог Г.Тейлор).
Физические и физико-химические свойства
Молекула имеет плоскую структуру (длины связей в нм):
азот в азотной кислоте четырёхвалентен, степень окисления +5.
азотная кислота - бесцветная, дымящая на воздухе жидкость,
концентрированная азотная кислота обычно окрашена в желтый цвет,
(высококонцентрированная HNO3 имеет обычно бурую окраску вследствие происходящего на свету процесса разложения:
4HNO3 == 4NO2 + 2H2O + O2 )
температура плавления -41,59°С,
кипения +82,6°С с частичным разложением.
растворимость азотной кислоты в воде неограничена. В водных растворах она практически полностью диссоциирует на ионы. С водой образует азеотропную смесь.
Химические свойства
При нагревании азотная кислота распадается по той же реакции.
4HNO3 == 4NO2 + 2H2O + O2 )
HNO3 как сильная одноосновная кислота взаимодействует:
а) с основными и амфотерными оксидами:
CuO + 2HNO3 = Cu(NO3)2 + H2O
ZnO + 2HNO3 = Zn(NO3)2 + H2O
б) с основаниями:
KOH + HNO3 = KNO3 + H2O
в) вытесняет слабые кислоты из их солей:
CaCO3 + 2HNO3 = Ca(NO3)2 + H2O + CO2
При кипении или под действием света азотная кислота частично разлагается:
4HNO3 = 4NO2 + O2 + 2H2O
Азотная кислота в любой концентрации проявляет свойства кислоты-окислителя, при этом азот восстанавливается до степени окисления от +4 до -3. Глубина восстановления зависит в первую очередь от природы восстановителя и от концентрации азотной кислоты.
Азотная кислота в любой концентрации проявляет свойства кислоты-окислителя, при этом азот восстанавливается до степени окисления от +4 до -3. Глубина восстановления зависит в первую очередь от природы восстановителя и от концентрации азотной кислоты.
Как кислота-окислитель, HNO3 взаимодействует:
а) с металлами, стоящими в ряду напряжений правее водорода:
Концентрированная HNO3
Cu + 4HNO3(60%) = Cu(NO3)2 + 2NO2 + 2H2O
Разбавленная HNO3
3Cu + 8HNO3(30%) = 3Cu(NO3)2 + 2NO + 4H2O
б) с металлами, стоящими в ряду напряжений левее водорода:
Zn + 4HNO3(60%) = Zn(NO3)2 + 2NO2 + 2H2O
3Zn + 8HNO3(30%) = 3Zn(NO3)2 + 2NO + 4H2O
4Zn + 10HNO3(20%) = 4Zn(NO3) 2 + N2O + 5H2O
5Zn + 12HNO3 = 5Zn(NO3) 2 + N2 + 6H2O д
4Zn + 10HNO3(3%) = 4Zn(NO3)2 + NH4NO3 + 3H2O
Все приведенные выше уравнения отражают только доминирующий ход реакции. Это означает, что в данных условиях продуктов данной реакции больше, чем продуктов других реакций, например, при взаимодействии цинка с азотной кислотой (массовая доля азотной кислоты в растворе 0,3) в продуктах будет содержаться больше всего NO, но также будут содержаться (только в меньших количествах) и NO2, N2O, N2 и NH4NO3.
Нитраты
HNO3 - сильная кислота. Её соли - нитраты - получают действием HNO3 на металлы, оксиды, гидроксиды или карбонаты. Все нитраты хорошо растворимы в воде.
Соли азотной кислоты - нитраты - при нагревании необратимо разлагаются, продукты разложения определяются катионом:
а) нитраты металлов, стоящих в ряду напряжений левее магния:
2NaNO3 = 2NaNO2 + O2
б) нитраты металлов, расположенных в ряду напряжений между магнием и медью:
4Al(NO3)3 = 2Al2O3 + 12NO2 + 3O2
в) нитраты металлов, расположенных в ряду напряжений правее ртути:
2AgNO3 = 2Ag + 2NO2 + O2
г) нитрат аммония:
NH4NO3 = N2O + 2H2O
Нитраты в водных растворах практически не проявляют окислительных свойств, но при высокой температуре в твердом состоянии нитраты - сильные окислители, например:
Fe + 3KNO3 + 2KOH = K2FeO4 + 3KNO2 + H2O - при сплавлении твердых веществ.
Соли азотной кислоты - нитраты - широко используются как удобрения. При этом практически все нитраты хорошо растворимы в воде, поэтому в виде минералов их в природе чрезвычайно мало; исключение составляют чилийская (натриевая) селитра и индийская селитра (нитрат калия). Большинство нитратов получают искусственно.
С азотной кислотой не реагируют стекло, фторопласт-4.
Производство азотной кислоты
Промышленное производство.
Современный способ её производства основан на каталитическом окислении синтетического аммиака на платино-родиевых катализаторах до смеси оксидов азота, с дальнейшим поглощением их водой
Промышленный способ получения HNO3 состоит из следующих основных стадий:
1. окисления аммиaка в NO в присутствии платино-родиевого
катализатора:
4NH3 + 5O2 = 4NO + 6H2O
2. окисления NO в NO2 на холоду под давлением (10 ат, 1 МПа):
2NO + O2 = 2NO2
3. поглощения NO2 водой в присутствии кислорода:
4NO2 + 2H2O + O2= 4HNO3
Массовая доля HNO3 в получаемом растворе составляет около 0,6.
Изредка применяемый дуговой способ получения азотной кислоты отличается только первой стадией, которая состоит в пропускании воздуха через пламя электрической дуги:
N2 + O2 = 2NO
Впервые азотную кислоту получили алхимики, нагревая смесь селитры и железного купороса:
Впервые азотную кислоту получили алхимики, нагревая смесь селитры и железного купороса:
4KNO3 + 2(FeSO4 · 7H2O) (t°) → Fe2O3 + 2K2SO4 + 2HNO3 + NO2 + 13H2O
Чистую азотную кислоту получил впервые Иоганн Рудольф Глаубер, действуя на селитру концентрированной серной кислотой:
KNO3 + H2SO4(конц.) (t°) → KHSO4 + HNO3
Дальнейшей дистилляцией может быть получена т. н. «дымящая азотная кислота», практически не содержащая воды.
- Это вещество было описано арабским химиком в VIII веке Джабиром ибн Хайяном (Гебер) в его труде «Ямщик мудрости», а с ХV века это вещество добывалось для производственных целей.
- Благодаря этому веществу русский учёный В.Ф. Петрушевский в 1866 году впервые получил динамит.
- Это вещество – прародитель большинства взрывчатых веществ (например, тротила, или тола).
- Это вещество является компонентом ракетного топлива, его использовали для двигателя первого в мире советского реактивного самолёта БИ – 1.
- Это вещество в смеси с соляной кислотой растворяет платину и золото, признанное «царём» металлов. Сама смесь, состоящая из 1-ого объёма этого вещества и 3-ёх объёмов соляной кислоты, называется «царской водкой».
Работа может использоваться для проведения уроков и докладов по предмету "Химия"
Готовые презентации по химии включают в себя слайды, которые учителя могут использовать на уроках химии для для изучения химических свойств веществ в интерактивной форме. Представленные презентации по химии помогут учителям в учебном процессе. На нашем сайте Вы можете скачать готовые презентации по химии для 7,8,9,10,11 класса.
1 слайд
Азотная кислота 1. Состав. Строение. Физические свойства 2. Классификация 3. Получение азотной кислоты 4. Химические свойства 5. Применение Тест Соли азотной кислоты

2 слайд
HNO3 Состав. Строение. Свойства. H O N O O - - степень окисления азота валентность азота +5 IV химическая связь ковалентная полярная Азотная кислота – бесцветная гигроскопичная жидкость, c резким запахом, «дымит» на воздухе, неограниченно растворимая в воде. tкип. = 83ºC.. При хранении на свету разлагается на оксид азота (IV), кислород и воду, приобретая желтоватый цвет: 4HNO3 = 4NO2 + O2 + 2H2O Азотная кислота ядовита.

3 слайд

4 слайд

5 слайд
Азотная кислота (HNO3) Классификация наличию кислорода: основности: растворимости в воде: летучести: степени электролитической диссоциации: кислородсодержащая одноосновная растворимая летучая сильная Азотная кислота по:

6 слайд
Получение азотной кислоты в промышленности NH3 NO NO2 HNO3 4NH3+ 5O2 = 4NO + 6H2O 2NO+O2 = 2NO2 4NO2 + 2H2O + O2 = 4HNO3 1. Контактное окисление аммиака до оксида азота (II): 2. Окисление оксида азота (II) в оксид азота (IV): 3. Адсорбция (поглощение) оксида азота (IV) водой при избытке кислорода

7 слайд
В лаборатории азотную кислоту получают действием концентрированной серной кислоты на нитраты при слабом нагревании. Составьте уравнение реакции получения азотной кислоты. NaNO3 + H2SO4 = NaHSO4 + HNO3

8 слайд
Химические свойства азотной кислоты 1. Типичные свойства кислот 2. Взаимодействие азотной кислоты с металлами 3. Взаимодействие азотной кислоты с неметаллами

9 слайд
Химические свойства азотной кислоты Азотная кислота проявляет все типичные свойства кислот. Перечислите свойства характерные для кислот. Кислоты взаимодействуют с основными и амфотерными оксидами, с основаниями, амфотерными гидроксидами, с солями. Составьте уравнения реакций азотной кислоты: 1 3 2 с оксидом меди (II), оксидом алюминия; c гидроксидом натрия, гидроксидом цинка; c карбонатом аммония, силикатом натрия. Рассмотрите реакции с т. зр. ТЭД. Дайте названия полученным веществам. Определите тип реакции. 3

10 слайд
2HNO3 + CuO = Cu(NO3)2 + H2O 1 2H+ + 2NO3– + CuO = Cu2+ + 2NO3– + H2O 2H+ + CuO = Cu2+ + H2O 6HNO3 + Al2O3 = 2Al(NO3)3 + 3H2O 6H+ + 6NO3– + Al2O3 = 2Al3+ + 6NO3– + 3H2O 6H+ + Al2O3 = 2Al3+ + 3H2O HNO3 + NaOH = NaNO3 + H2O H+ + NO3– + Na+ + OH– = Na+ + NO3– + H2O H+ + OH– = H2O 2 2HNO3 + Zn(OH)2 = Zn(NO3)2 + 2H2O 2H+ + 2NO3– + Zn(OH)2 = Zn2+ +2NO3– + 2H2O 2H+ + Zn(OH)2 = Zn2+ + 2H2O

11 слайд
3 2HNO3 + (NH4)2CO3 = 2NH4NO3 + CO2 + H2O 2H+ + 2NO3– + 2NH4+ + CO22– = 2NH4+ +2NO3– + CO2 + H2O 2H+ + CO22– = CO2 + H2O 2HNO3 + Na2SiO3 = ↓H2SiO3 + 2NaNO3 2H+ + 2NO3– + 2Na+ + SiO32– = ↓H2SiO3 + 2Na+ + 2NO3– 2H+ + SiO32– = ↓H2SiO3 Активные кислоты вытесняют слабые летучие или нерастворимые кислоты из растворов солей.

12 слайд
Взаимодействие азотной кислоты с металлами Как реагируют металлы с растворами кислот? Металлы, стоящие в ряду активности до водорода, вытесняют его из кислот. Металлы, стоящие после водорода из кислот его не вытесняют, т.е. не взаимодействуют с кислотами, не растворяются в них. Особенности взаимодействия азотной кислоты с металлами: 1. Ни один металл никогда не выделяет из азотной кислоты водород. Выделяются разнообразные соединения азота: N+4O2, N+2O, N2+1O, N20, N–3H3 (NH4NO3) 2. С азотной кислотой реагируют металлы, стоящие до и после водорода в ряду активности. 3. Азотная кислота не взаимодействует с Au, Pt 4. Концентрированная азотная кислота пассивирует металлы: Al, Fe, Be, Cr, Ni, Pb и другие (за счет образования плотной оксидной пленки). При нагревании и при разбавлении азотной кислоты данные металлы в ней растворяются. опыт опыт опыт N–3H4+ N20 N2+1O N+2O N+4O2 концентрация кислоты активность металлов

13 слайд

14 слайд
Составьте уравнение реакции взаимодействия концентрированной азотной кислоты с ртутью. Рассмотрите реакцию с т. зр. ОВР. 4HN+5O3 + Hg0 = Hg+2(NO3)2 + 2N+4O2 + 2H2O N+5 + 1e → N+4 1 2 Hg0 – 2e → Hg+2 2 1 HNO3 (за счет N+5) – окислитель, процесс восстановления; Hg0– восстановитель, процесс окисления.

15 слайд
Допишите схемы реакций: Рассмотрите превращения в свете ОВР 1) HNO3(конц.) + Cu → Cu(NO3)2 + … + H2O 2) HNO3(разб.) + Cu → Cu(NO3)2 + … + H2O 1) HN+5O3(конц.) + Cu0 = Cu+2(NO3)2 + N+4O2 + H2O 2 2 N+5 + 1e → N+4 1 2 Cu0 – 2e → Cu+2 2 1 2) HN+5O3(конц.) + Cu0 = Cu+2(NO3)2 + N+2O + H2O 3 3 4 2 8 N+5 + 3e → N+2 3 2 Cu0 – 2e → Cu+2 2 3 восстановление окисление восстановитель окислитель 4 восстановление окисление окислитель восстановитель

16 слайд

17 слайд
Взаимодействие азотной кислоты с неметаллами Окисляет неметаллы до соответствующих кислот. Концентрированная (более 60%) азотная кислота восстанавливается до NO2 , а если концентрация кислоты (15 – 20%), то до NO. HNO3 + С → СO2 + H2O + NO2 N+5 + 1e → N+4 1 4 С0 – 4e → С+4 4 1 4 4 2 HNO3 + P → H3PO4 + NO2 + H2O N+5 + 1e → N+4 1 5 P0 – 5e → P+5 5 1 5 2 5 HNO3 + P + H2O → H3PO4 + NO N+5 + 3e → N+2 3 5 P0 – 5e → P+5 5 3 3 5 3 5 Азотная кислота как сильный окислитель Расставьте в схемах коэффициенты методом электронного баланса. HNO3 (за счет N+5) – окислитель, пр. восстановления C – восстановитель, процесс окисления HNO3 (за счет N+5) – окислитель, пр. восстановления P – восстановитель, процесс окисления HNO3 (за счет N+5) – окислитель, пр. восстановления P – восстановитель, процесс окисления опыт опыт

18 слайд

19 слайд

20 слайд
Применение азотной кислоты 1 5 4 6 2 3 Производство азотных и комплексных удобрений. Производство взрывчатых веществ Производство красителей Производство лекарств Производство пленок, нитролаков, нитроэмалей Производство искусственных волокон 7 Как компонент нитрующей смеси, для траления металлов в металлургии

21 слайд
Соли азотной кислоты Как называются соли азотной кислоты? нитраты Нитраты K, Na, NH4+ называют селитрами Составьте формулы перечисленных солей. KNO3 NaNO3 NH4NO3 Нитраты – белые кристаллические вещества. Сильные электролиты, в растворах полностью диссоциируют на ионы. Вступают в реакции обмена. Каким способом можно определить нитрат-ион в растворе? К соли (содержащей нитрат-ион) добавляют серную кислоту и медь. Смесь слегка подогревают. Выделение бурого газа (NO2) указывает на наличие нитрат-иона.
23 слайд
Кристаллическое вещество белого цвета. Температура плавления 169,6 °C, при нагреве выше этой температуры начинается постепенное разложение вещества, а при температуре 210°С происходит полное разложение. Нитрат аммония

24 слайд
При нагревании нитраты разлагаются тем полнее, чем правее в электрохимическом ряду напряжений стоит металл, образующий соль. Li K Ba Ca Na Mg Al Mn Zn Cr Fe Co Sn Pb Cu Ag Hg Au нитрит + О2 оксид металла + NO2 + O2 Ме + NO2 + O2 Составьте уравнения реакций разложения нитрата натрия, нитрата свинца, нитрата серебра. 2NaNO3 = 2NaNO2 + O2 2Pb(NO3)2= 2PbO + 4NO2 + O2 2AgNO3 = 2Ag + 2NO2 + O2

25 слайд
1. Степень окисления азота в азотной кислоте равна: А) +5; Б) +4; В) -3. А 2. При взаимодействии с какими веществами азотная кислота проявляет особые свойства, отличающие её от других кислот: А) основными оксидами; Б) металлами; В) основаниями. Б 3. В окислительно-восстановительной реакции азотная кислота может участвовать в качестве: А) окислителя; Б) восстановителя; В) окислителя и восстановителя. А 4. Какое из данных соединений азота называют чилийской селитрой: А) нитрат калия; Б) нитрат кальция; В) нитрат натрия; В 5. Запишите уравнение взаимодействия меди с концентрированной азотной кислотой. Коэффициент перед формулой кислоты равен: А) 2; Б) 4; В) 1. Б 6. Какое из перечисленных веществ не реагирует с разбавленной азотной кислотой: А) медь; Б) гидроксид натрия; В) бромид натрия. В 7. Азотную кислоту получают в три стадии, окисляя атом азота по следующей схеме: А) N–3 →N+2 →N+4 → N+5 Б) N–3 →N0 →N+4 → N+5 В) N0 →N+2 →N+4 → N+5 А
Азотная кислота и её соли
Подготовила учитель химии КОУ ВО «ЦЛПДО» Саврасова М.И.

Вспомните!
- Какие степени окисления проявляет азот в своих оксидах?
- Какие окислы азота вы знаете?
- Расскажите о N2O, NO, NO2?
- Какое из этих соединений азота наиболее важное с точки зрения хозяйственного производственного значения?


- Изучение свойств азотной кислоты,
- Её значения в хозяйственной деятельности человека.

Строение молекулы
HNO3 – молекулярная формула

Физические свойства азотной кислоты
- Рассмотрите выданные вам образцы азотной кислоты.
- Проверьте цвет, прозрачность, растворимость в воде. Запишите наблюдения в тетрадь.

Химические свойства азотной кислоты
- Очень сильная кислота
- В водном растворе диссоциирует:
- Н NO3 ↔NO3 + H
- Взаимодействует:
- С металлами
- Cu +4HNO3 = Cu(NO3)2 +2NO2 +2H2O
- С оксидами металлов:
- CuO + 2HNO3= Cu(NO3)2 +H2O
- С гидроксидами металлов
- Cu(OH)2 + 2HNO3 = Cu(NO3)2 + 2H2O

Особые свойства
- Cu +4HNO3 = Cu(NO3)2 +2NO2 +2H2O
- При нагревании выделяется бурый газ, он ядовит для человека.
Качественная реакция на нитрат ионы

Производство азотной кислоты
- Окисление азота воздуха.
- Доокисление оксида азота+2 в оксид азота +4
- Получение азотной кислоты.
Составьте уравнения соответствующих реакций.

Применение азотной кислоты
Взрывчатые вещества
Лекарства
Азотная кислота
Искусственные волокна
Красители
Удобрения

Нитраты
- NaNO3
- NH4NO3
- Ca (NO3)2
- Соли азотной кислоты называются ещё селитрами. Они применяются при производстве спичек, пороха, удобрений.

Закрепление
- 2KNO3 →2KNO2 +O2
- Качественная реакция на нитраты.
- Решите правильно или неправильно предложенное Вам выссказывание:
- 1. Азотная кислота тяжёлая плохо растворимая в воде жидкость.
- 2.Азотная кислота жёлтоватая жидкость хорошо растворимая в воде.

Закрепление
- 3. Азотная кислота образует соли – нитриты.
- 4. Азотная кислота образует соли- нитраты.
- 5. В азотной кислоте азот +5.
- 6. В азотной кислоте азот +4.
- 7.Азотная кислота не реагирует с металлами после водорода.

Закрепление
8. Азотная кислота не реагирует с любыми металлами.
9. Азотная кислота реагирует с оксидами металлов.
10. Азотная кислота реагирует с основаниями.
11.Азотная кислота реагирует с солями.
12. Азотную кислоту можно обнаружить по реакции её с медью.
13. Азотную кислоту можно узнать по взаимодействию её с углём.

Проверьте свои знания:
- Правильные ответы:
- 1,4,5, 9,10,11,12.

Домашнее задание
§29 упражнения 1-4